Aide à la relecture : Chloé Jarroir, Marguerite Dontenwille, Robin Vervaeke
Abréviations :
- ASI : Articulations Sacro-Iliaques
- DSI : Douleurs en lien avec les articulations Sacro-Iliaques
- DPPG : Douleurs Pelviennes Postérieures en lien avec la Grossesse (supposément attribuées aux ASI)
- ECR : Essai Contrôlé Randomisé
- ODI : Oswestry Disability Index
Maintenant que nous avons passé en revue les données relatives à l’efficacité de la kinésithérapie, des infiltrations et de la chirurgie, il est temps de conclure et de se demander comment intégrer ces données dans notre pratique clinique ?
CONCLUSION : « tout ce qu’on sait c’est qu’on ne sait rien »
Les stratégies thérapeutiques disponibles pour le traitement des DSI sont variées (Figure 11). Cependant, les preuves existant pour chacune de ces interventions sont généralement de qualité médiocre. Quelques preuves de qualité satisfaisante sont disponibles mais résultent de rares études qui manquent de cohérence externe ; autrement dit : les résultats restent à être confirmés.
N.B. : Pour rappel, quand les preuves sont de faible qualité, cela signifie que l’on ne peut pas faire confiance aux résultats : ces résultats auraient très bien pu être les mêmes, ou bien être complètement différents si la rigueur méthodologique avait été meilleure. Autrement dit, n’ayant pas la certitude que l’effet de l’intervention obtenu par une méthodologie peu contraignante n’est pas juste un artefact lié à ce manque de rigueur, on ne peut décemment pas proposer au patient ces interventions, et a fortiori si elles sont invasives ou avec des effets secondaires indésirables.
Et finalement, il est difficile au regard des preuves existantes de hiérarchiser les différentes interventions disponibles en fonction de leur efficacité.
Nous pouvons néanmoins retenir que la kinésithérapie a un rôle à jouer pour améliorer certes modestement l’incapacité et la qualité de vie des patients souffrant de DSI persistant depuis plusieurs années et ce, sans améliorer pour autant significativement la douleur. A cet égard, une approche majoritairement active à base d’exercices est requise. La thérapie manuelle peut être proposée comme adjuvant. Cependant, il n’est pas possible de déterminer à partir des données probantes disponibles quels exercices et quelles techniques de thérapie manuelle sont particulièrement pertinentes ici. On ignore également à quelle posologie la kinésithérapie doit être réalisée (fréquence, intensité, durée de la réhabilitation).
Dans la perspective d’une approche conservatrice multimodale, les infiltrations peuvent être envisagées (à condition d’être réalisées sous contrôle scopique), car elles bénéficient de quelques preuves d’une efficacité significative à court terme, contrairement à la dénervation radiofréquence.
Enfin, la chirurgie semble être une option pertinente pour presque tous les critères de jugement (douleur, incapacité, qualité de vie …) et pourra être discutée avec le patient et ses autres référents médicaux en cas d’absence de bénéfice significatif avec la kinésithérapie dans un délai d’au moins 6 mois qui devra être déterminé au préalable et de façon collégiale.
Néanmoins, chacune de ces modalités doit encore faire ses preuves.
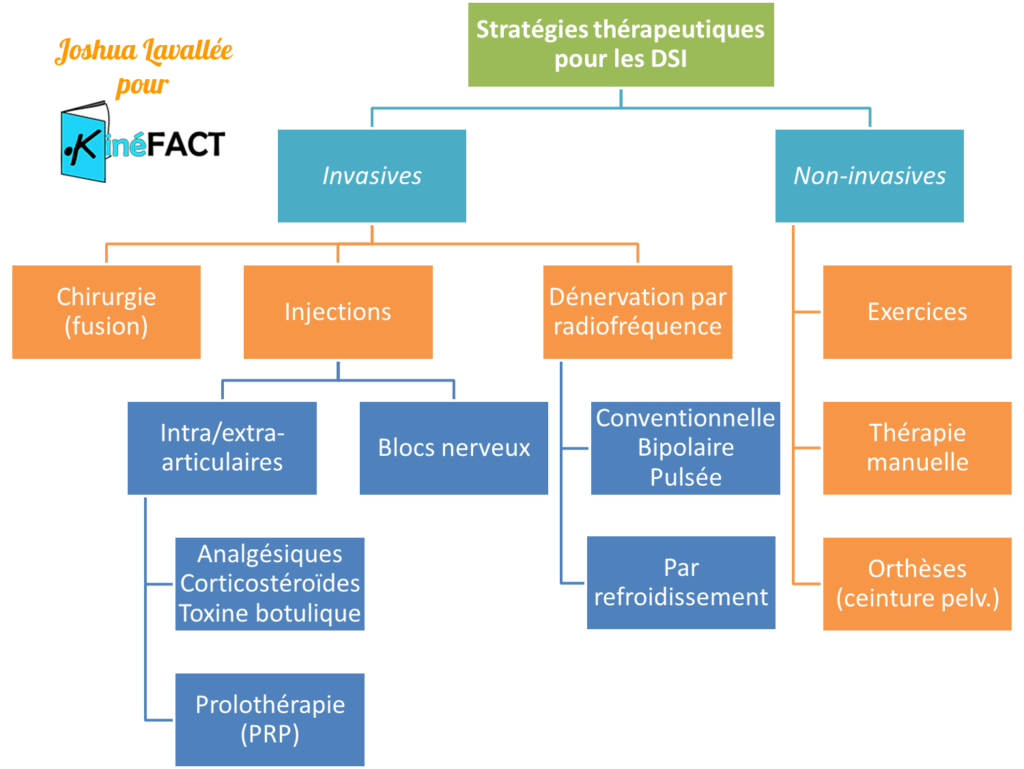
Figure 11 :
Synthèse des principales stratégies thérapeutiques pour la prise en charge des DSI
Bon, nous voilà bien avancés.
Alors que faire en pratique courante de kinésithérapie ?
Ce n’est pas à moi de vous dire quoi faire dans votre pratique. Mais on peut, à défaut de mieux, se tourner vers les avis d’experts. Mais peut-on faire confiance à leur opinion ?
Face au manque de consensus scientifique (que nous avons pu largement constater !) et à la diversité des opinions de la part des différents groupes de recherche, une étude ayant réuni un collège d’experts (chercheurs sur le sujet, et cliniciens), issus de différentes disciplines en lien avec le champ musculosquelettique (5 kinés, 7 médecins, 1 ostéo, 1 anatomiste), reconnus sur la question des DSI (dont Laslett, Gütke, Mens, Lee, Vleeming, autant de noms qui devraient vous être familiers si vous m’avez lu depuis le début de ces séries d’articles sur les DSI) a cherché à développer un modèle collaboratif de compréhension des DSI (Figure 12).
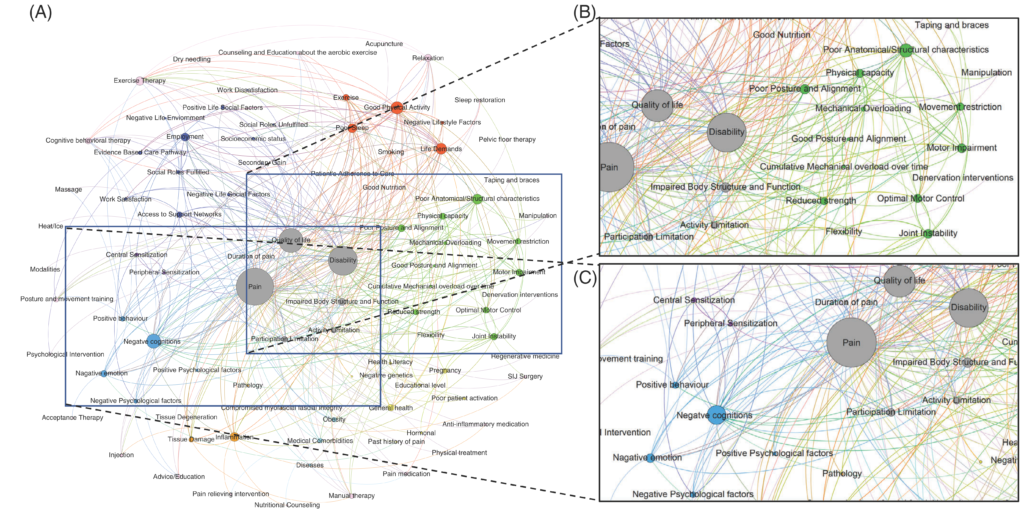
Figure 12 :
Méta-modèle collaboratif de compréhension des DSI
Chaque expert devait proposer les différents facteurs qui contribuent selon lui aux DSI (répartis par catégories d’après la CIF : hygiène de vie, biomécaniques, comorbidités, psychologiques, etc.) et pondérer ces composantes en fonction de l’importance de leur contribution dans le tableau des DSI. Cela résulte en une modélisation de leur représentation du problème structurée en réseau (« carte mentale ») permettant de rendre compte de l’interdépendance des différents facteurs (Figure 13). Les cartes mentales de chaque expert ont ensuite été combinées dans une méta-modélisation, permettant ainsi d’identifier les concepts fondamentaux qui sous-tendent l’opinion des experts ainsi que leur importance relative, résultant en une synthèse de l’opinion collective des contributeurs. Chacune des modélisations individuelles avaient le même « poids » dans le méta-modèle, les auteurs n’ayant pas le moyen d’en pondérer la crédibilité.
– – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – – –
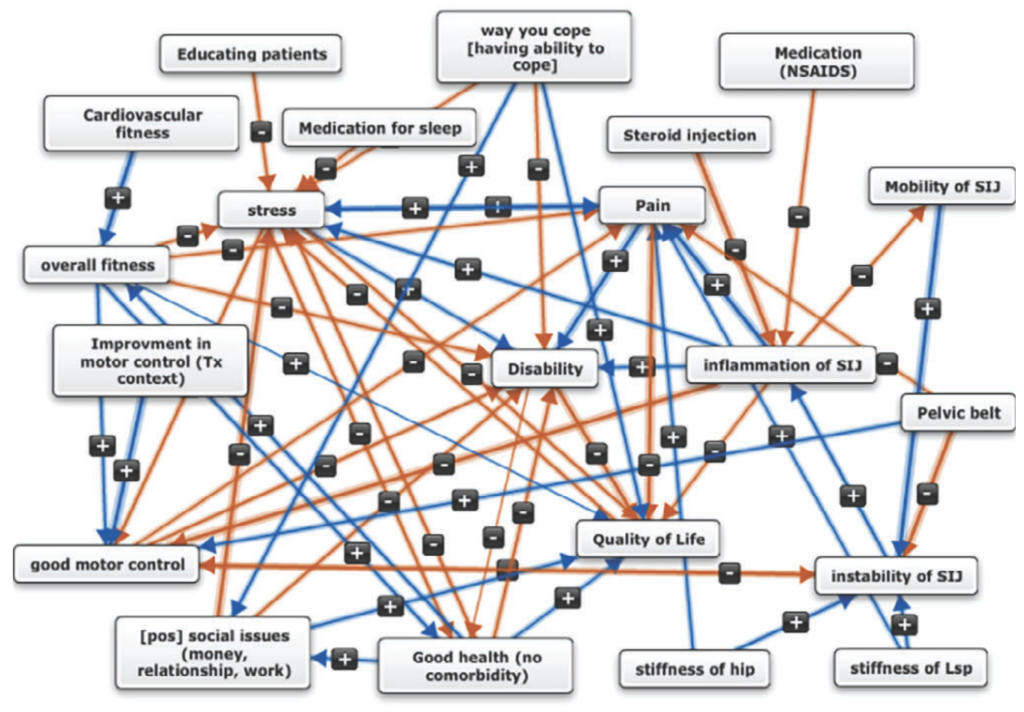
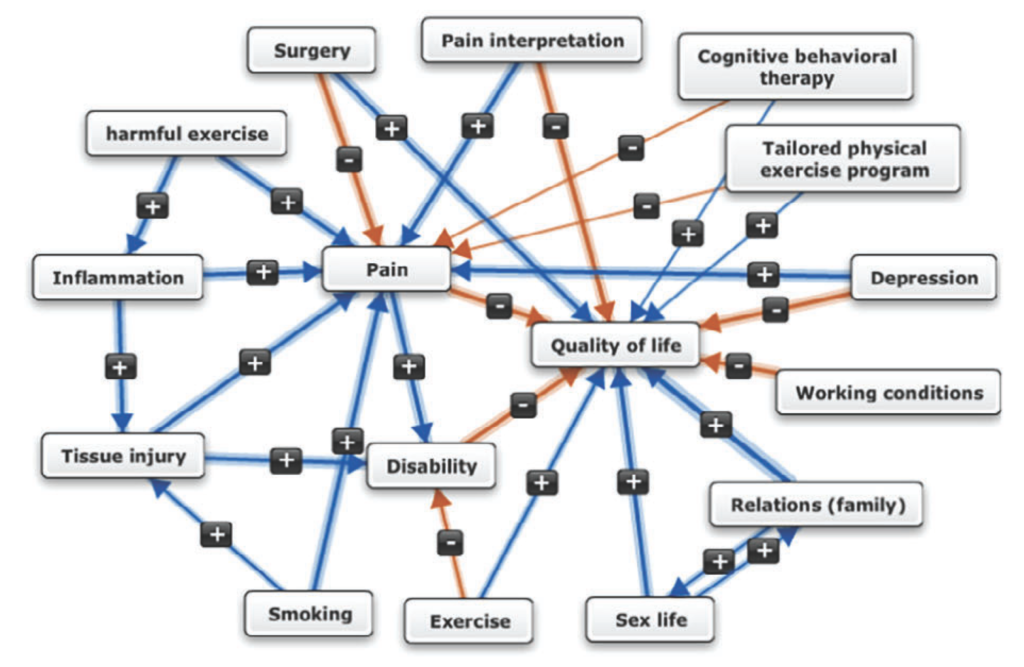
Figure 13 :
2 exemples de cartes mentales, illustrant la différence de complexité possible de la représentation du même problème par 2 experts sur ce problème
Au final, les auteurs mettent en évidence que ce méta-modèle a un biais clair vers une compréhension biomécanique des DSI avec 3 facteurs émergents comme contributeurs principaux, à savoir : « caractéristiques anatomiques ou structurelles » (e.g. : scoliose), « déficiences motrices » (contrôle neuro-moteur) et « mauvaise posture / mauvais alignement » (e.g. : différence de longueur des membres inférieurs). Autrement dit : dans la compréhension collective des DSI, les facteurs biomécaniques seraient prédominants.
Néanmoins, la catégorie « psychologie » était la 4e catégorie parmi celles considérées comme les plus importantes dans la contribution aux DSI, dont le facteur côté comme le plus contributif était les cognitions (attentes, croyances, perceptions autour de la douleur). En outre, des facteurs appartenant à la catégorie « style de vie » faisaient partie du « top 10 » des facteurs les plus contributifs, avec des paramètres tels qu’une bonne activité physique et un mauvais sommeil.
De façon assez surprenante, le facteur « grossesse » ne ressortait pas de ce modèle comme un des facteurs les plus contributifs, ce qui est assez inattendu au regard de la prévalence élevée de DSI en lien avec la grossesse (DPPG) et de l’attention particulière de certains des experts dans cette population précise. La raison à cela n’est pas clairement identifiée par les auteurs, mais ils suggèrent que les experts ont accordé plus d’importance à des facteurs associés à la grossesse (hypermobilité articulaire par exemple) qu’à la grossesse elle-même.
Ce modèle permettant également de réaliser des prédictions sur le(s) traitement(s) le(s) plus approprié(s) qui en découle(nt), celles-ci ont été comparées aux résultats des essais thérapeutiques existant (dont vous connaissez déjà les résultats après avoir lu cet article déjà beaucoup trop long) afin de tester la validité dudit modèle.
Les résultats de ce méta-modèle, qui synthétise l’opinion collective des différents contributeurs, suggèrent que les interventions prédites comme les plus efficaces (Figure 14) pour la réduction de la douleur sont les injections, les exercices et la chirurgie. Les exercices, les thérapies cognitives et comportementales (TCC) et l’éducation étaient anticipées comme les plus efficaces pour réduire l’incapacité. Enfin, les exercices, les TCC et la chirurgie étaient attendues comme les plus efficaces pour améliorer la qualité de vie. Or, comme nous avons pu le voir tout au long de cet article, et les auteurs le confirment, les prédictions du modèle ne collent pas avec les meilleures données disponibles pour ces thérapeutiques !
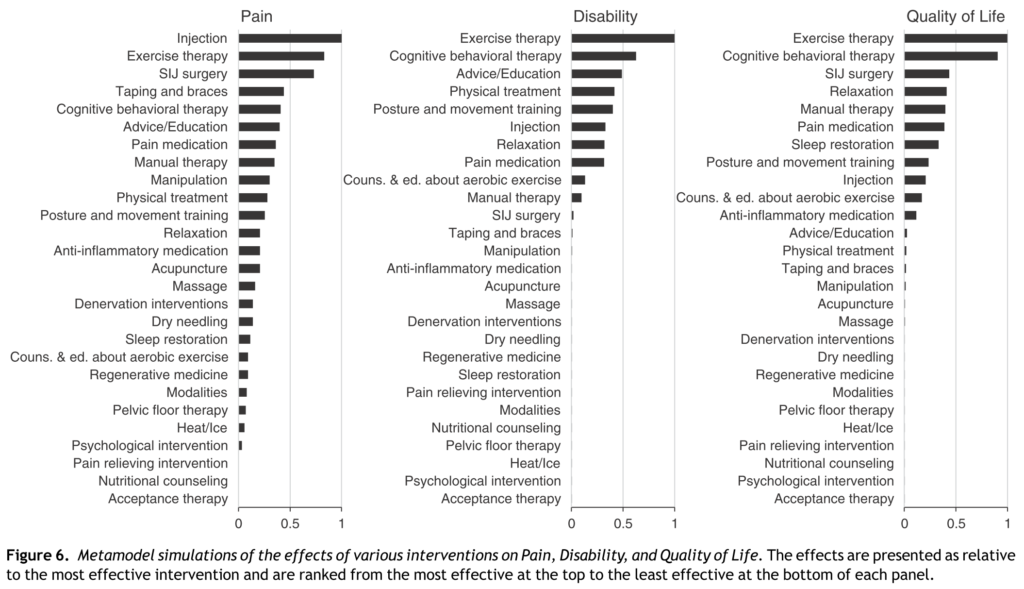
Figure 14 :
Résultats des simulations des meilleurs thérapeutiques pour chaque critère de jugement
(douleur, incapacité et qualité de vie)
Le modèle met donc en évidence un écart entre l’efficacité prédite des différentes interventions et les résultats des données disponibles.
On peut se demander alors dans quelle mesure cette discordance invalide le méta-modèle :
- ou bien la concordance entre les prédictions des meilleurs traitements et les meilleures preuves disponibles pour ces traitements est médiocre parce que le modèle est invalide et l’opinion collective des experts est erronée, auquel cas ces résultats doivent motiver un changement radical de paradigme en admettant que l’importance des facteurs biomécaniques a été largement surestimée ;
- ou bien parce que la qualité des « meilleures » preuves disponibles reste globalement faible (ce qui veut juste dire qu’on ne peut pas faire aveuglément confiance aux résultats des études, pas que les résultats sont nécessairement faux).
Ces deux hypothèses ne sont bien sûr pas mutuellement exclusives.
Quoiqu’il en soit : d’importants efforts de recherche doivent encore être fournis tant sur le cadre conceptuel des DSI, que sur la qualité des recherches effectuées.
Alors peut-on faire confiance aux experts ?
Manifestement pas collectivement ! (sinon le méta-modèle permettrait des prédictions justes)
Peut-on leur faire confiance individuellement alors ?
Etant donné l’hétérogénéité des opinions, ils ne peuvent pas tous avoir raison en même temps (sinon le méta-modèle permettrait des prédictions justes) ! Donc, soit ils ont TOUS « tort », soit seuls quelques experts (ou bien un seul) ont « raison » dans le lot. Dans tous les cas, il ne nous est pas possible de déterminer qui a tort et qui a raison, et donc qui croire !
Comme quoi, ce n’est pas parce qu’on est expert qu’on a raison !
Cette situation peut nous pousser à vouloir choisir arbitrairement l’expert à qui on accorderait notre confiance. Or, dans une telle situation, le risque est que nous nous trompions d’expert. Le risque est même que nous nous trompions dans le fait de vouloir accorder notre confiance à un « expert » (oui je mets des guillemets maintenant du coup). Peut-être au final est-il plus sage en l’état actuel des connaissances scientifiques sur ce sujet de ne pas chercher à indexer notre propre expertise (clinique) à celle d’un « expert ». Peut-être la position la plus raisonnable d’adopter pour l’instant est la suivante :
- faire du mieux qu’on peut (en pratique clinique) avec le mieux dont on dispose (en termes de connaissances scientifiques) ;
- suspendre son jugement : admettre qu’on ne peut pas encore conclure définitivement, rester ouvert et s’informer régulièrement des nouvelles données issues de la recherche, mais sans pour autant chercher à les implémenter trop vite dans notre pratique et attendre patiemment qu’elles soient suffisamment solides.
Mais faisons attention à ne pas tomber dans le sophisme de l’appel à l’ignorance combiné à un sophisme de la solution parfaite ! Ce n’est pas parce qu’on ne peut pas conclure sur quelles sont les meilleures stratégies dans l’absolu et ce n’est pas parce que les preuves disponibles ne sont pas de qualité élevée que cela justifie de faire comme on le « sent ».
Veillons aussi à ne pas jeter le bébé avec l’eau du bain. Quelques preuves sont disponibles, et même si leur validité est discutable, nous devrions baser nos décisions cliniques sur la base de preuves en tenant compte de l’incertitude qui les entoure. Il nous revient ensuite, avec notre expertise clinique, de déterminer comment adapter ces preuves en fonction de chaque patient. Cette approche est celle de l’Evidence-Based Pratice (EBP) (Figure 12).
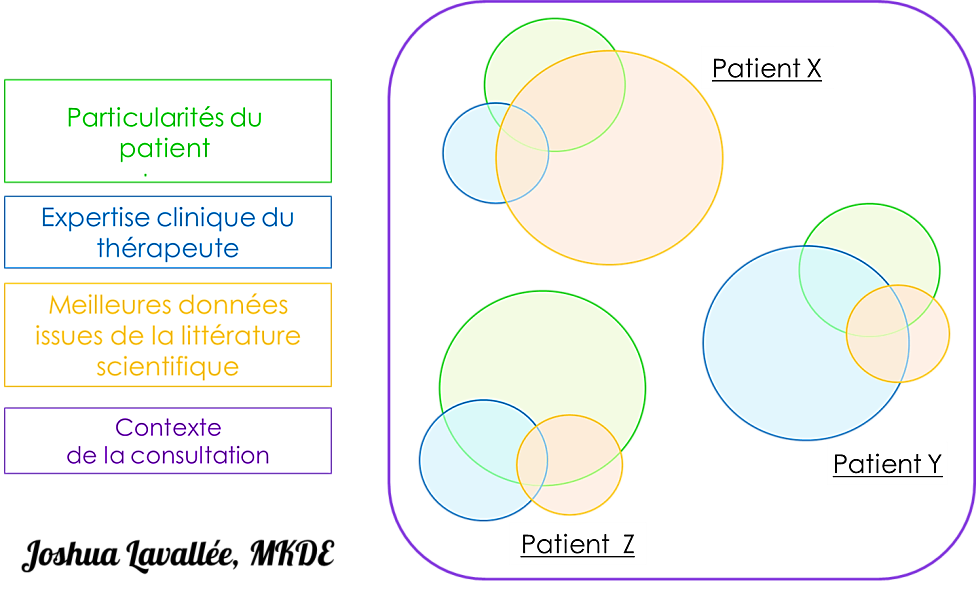
Figure 12 :
L’EBP, une modélisation graphique des dimensions en jeu dans une décision clinique centrée sur le patient. La variation de géométrie illustre la variation relative de l’importance de ces « ingrédients décisionnels » en fonction de chaque situation, et constitue une proposition de représentation de l’EBP mettant l’accent sur son caractère dynamique et adaptatif.
« Faire du mieux que je peux avec le mieux que j’ai » :
BON ALORS, à défaut, je peux toujours vous soumettre modestement la façon dont, en l’état actuel de mes connaissances sur la question après 3 séries d’articles et un panorama pas encore tout à fait exhaustif de la littérature sur le sujet, je serais susceptible de procéder avec des patients dont l’hypothèse d’une DSI chronique non-rhumatismale ou d’une DPPG non-résolue à plus de 18 mois semble être la plus pertinente à l’issue d’un processus de différenciation clinique rigoureux et exhaustif.
ATTENTION :
Si j’ai montré que l’opinion des experts était inconsistante et ne pouvait être crue, ce n’est pas pour que vous croyiez plus naïvement à la mienne, bien au contraire.
Mon opinion n’a pas vocation à avoir valeur de vérité et est susceptible d’évoluer.
Veillez à rester critique et à ne pas prendre mon avis pour argent comptant.
D’abord, EVALUER (encore) : évaluer la sévérité à l’aide d’échelle(s) validée(s) (telles que l’Oswestry, l’EIFEL, le QBPDS, le DALLAS) et de test(s) fonctionnel(s) (qui pourront servir de marqueurs du suivi de l’évolution au fil de la prise en charge), afin de faciliter la communication avec les autres soignants, et d’aider à prioriser le choix des stratégies thérapeutiques en concertation avec eux et le patient. Je chercherais également à identifier si possible les activités qui augmentent les symptômes afin de conseiller éventuellement le patient sur une adaptation ou à défaut, un évitement temporaire de ces activités si cela me semble pertinent pour réduire la sévérité des symptômes, avant d’en proposer une ré-exposition graduelle et progressive (« calm shit down, built back up »). Ce processus peut être l’opportunité de montrer au patient que certaines activités ne sont pas nécessairement « mauvaises » pour lui mais seulement qu’un dosage spécifique est requis, luttant ainsi contre le cercle vicieux de peur-évitement. Dans cette perspective, je ne pense pas qu’il n’y ait pas de « bons » ou de « mauvais » exercices pour les DSI : ce qui compte c’est la capacité de l’exercice à générer des forces dans les ASI, et la capacité du thérapeute à choisir et à adapter les multiples exercices à sa disposition judicieusement au fil de la prise en charge.
La thérapie manuelle, manipulative ou non, a toute sa place dans une prise en charge multidimensionnelle afin d’aider à moduler les symptômes (aucune donnée expérimentale ne soutient la capacité à affecter la position ou la mobilité des ASI par un traitement manuel) et ainsi aider le patient à bouger, mais aussi à lutter contre la kinésiophobie et le catastrophisme (« vous pouvez aller mieux et le mouvement peut vous y aider ») (Figure 13). Elle peut être également envisagée comme le premier jalon de la ré-exposition graduelle à un mouvement ou une activité.
Enfin, du reconditionnement musculaire et aérobie global sera proposé dans une perspective salutogène, en fonction de la réponse symptomatique du patient monitorée au cours et entre les séances.
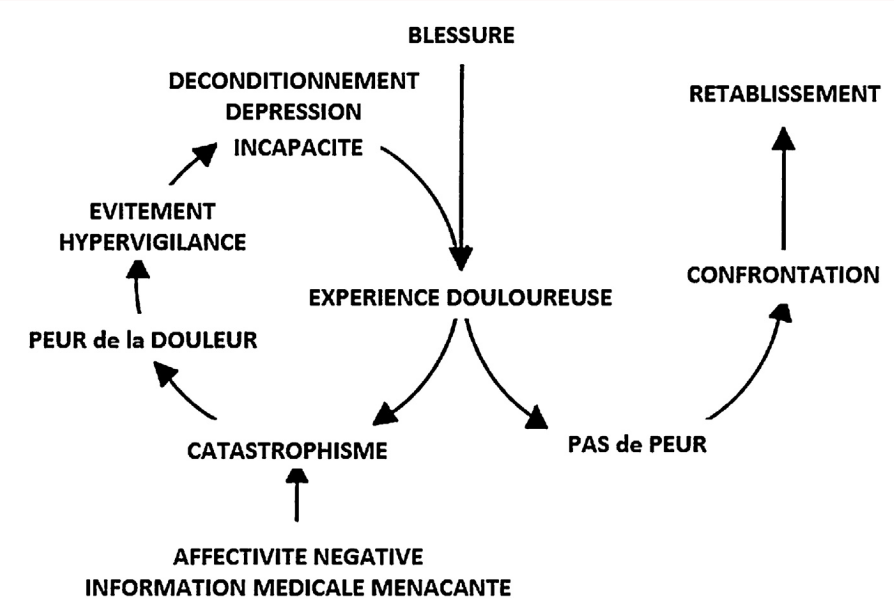
Figure 13 :
Cercle vicieux de peur-évitement (Vlaeyen 2006), issu de [17]
Le port d’une ceinture pelvienne sera testé par principe afin de déterminer si elle permet de créer ou d’élargir une fenêtre thérapeutique pour la kinésithérapie. Cela reste spéculatif, mais il est possible qu’un sous-groupe spécifique de patients souffrant de DSI réponde plus favorablement aux contraintes en compression. Auquel cas, on peut envisager que lorsqu’un patient répond positivement au test de la ceinture (amélioration de la douleur et/ou des marqueurs fonctionnels avec le port de la ceinture), des exercices visant à produire plus spécifiquement des forces de compression dans les ASI puissent être intégrés au programme de réhabilitation.
S’il est difficile à cause de la sévérité des symptômes d’obtenir une fenêtre thérapeutique suffisante, des stratégies infiltratives peuvent être discutées avec le patient et le médecin. Si le patient a déjà reçu une injection diagnostique positive (intra-articulaire, sous contrôle fluoroscopique, avec une amélioration d’au moins 80% des douleurs, si possible contrôlée), rappelons-nous qu’il n’est pas clair au regard de la littérature que celle-ci prédise une réponse favorable à une injection thérapeutique, bien que cela puisse sembler contre-intuitif. Cette donnée doit être fournie au patient afin de lui permettre de prendre une décision éclairée quant à cette intervention.
Tout au long de la prise en charge, il sera pertinent d’embrasser les dimensions cognitives, affectives et comportementales de l’expérience de la douleur par le patient car elles peuvent en moduler la sensibilité, et donc la sévérité. Permettre au patient de se rassurer quant à la gravité de sa situation et à l’innocuité du mouvement est susceptible d’ouvrir une autre fenêtre thérapeutique en le rendant plus à même d’accepter le mouvement et d’en avoir une expérience plus positive. De multiples stratégies sont envisageables (attitude positive, réassurance cognitive, exercices douloureux …) mais ce n’est pas le sujet ici. Néanmoins, à cet égard, le discours qui habillera nos choix thérapeutiques ainsi que nos différentes stratégies sera déterminant [18 – 25].
« Tout ce qui change l’évaluation du danger par le cerveau change la douleur »
L. Moseley
Enfin, en cas d’échec d’amélioration objective et satisfaisante pour le patient par la kinésithérapie dans un délai qui devra être discuté dès le départ avec celui-ci et avec ses autres soignants, une arthrodèse pourra être envisagée (à condition qu’une injection diagnostique positive ait été obtenue au préalable). En revanche, je déconseillerais à un patient de subir une dénervation par radiofréquence.
POSTAMBULE
Bien, il est temps pour moi de tirer ma révérence après près de 2 années passées sur ce sujet. Néanmoins (oui je m’étends encore mais vous n’êtes plus à ça près n’est-ce pas ?), j’aimerais vous laisser avec quelques notions que j’ai pu retirer personnellement au-delà des données factuelles :
« C’est toujours plus complexe que ce qu’on pense »
- Si ce travail m’a appris une chose c’est que lorsqu’on s’intéresse à « comment on sait ce qu’on sait », autrement dit « comment s’est construite notre connaissance », on s’aperçoit que rien n’est jamais aussi tranché et tout est toujours plus complexe que ce qu’on pourrait croire a priori. La conséquence de cela est que l’on devrait toujours se retenir d’être trop convaincu par ce qu’on pense être vrai, et donc on devrait éviter d’être trop attaché à nos croyances et à nos opinions du moment, afin d’être en mesure le jour venu où les connaissances évolueront de pouvoir changer notre fusil d’épaule et se ranger à la position la mieux argumentée. Du moins, si l’honnêteté intellectuelle et la volonté d’appréhender le Réel tel qu’il est et non pas tel que l’on voudrait qu’il soit sont des objectifs que l’on souhaite respecter (ce qui serait pertinent avec notre rôle de soignants et de proposer à nos patients les meilleurs soins).
- Le corolaire de cela est que l’on devrait se méfier des vendeurs de simplicité. Si vous avez eu le courage de me lire jusqu’ici (et je m’en sens sincèrement honoré), j’espère avoir réussi à transmettre l’idée que tout n’est que nuance et contexte : une donnée ne devrait jamais être comprise en dehors du cadre théorique et méthodologique dans lequel elle a été établie. Ainsi, les « recettes » ont peu de chances d’approcher un tant soit peu la réalité d’un problème.
- La Science peut être décevante. Imaginez ma frustration de ne pas pouvoir tirer de conclusion affirmée après 2 ans d’enquête sur ce sujet. Pourtant je sais bien que « c’est le jeu ma pauvre lucette ». En effet la méthode scientifique ne peut matériellement pas nous apporter toutes les réponses qu’on voudrait dès aujourd’hui. Il faut donc que nous soyons vigilants quant à nos attentes envers la Science : il s’agirait de ne pas lui demander l’impossible. Et ce d’autant plus que la recherche dans la médecine musculosquelettique est encore jeune !
- Cependant, ma déception a été la plus forte en m’apercevant que, sur ce sujet au moins, le jeu de la méthode scientifique se base (trop) souvent sur un « téléphone arabe » abscons. Avant de tenir pour vraie une connaissance, nous devrions faire l’effort de remonter la piste de son établissement afin de s’assurer de sa validité. Nos collègues de Le Temps D’un Lapin, ont magistralement illustré ce point dans deux titres consacrés à la lombalgie non-spécifique que je ne peux que vous recommander d’écouter :
- Au final, lorsque nous nous penchons sur un sujet de science, il faut nous attendre à entrer dans un dédale de nuances et de complexité dont nous ne ressortirons pas avec des réponses tranchées. Il me paraît donc judicieux d’adopter une posture de suspension de nos attentes et de suspension de notre jugement afin d’être en mesure d’accueillir de façon neutre la réalité de l‘état actuel des connaissances scientifiques.
MERCI PROFONDÉMENT DU TEMPS QUE VOUS AVEZ CONSACRÉ À ME LIRE.
Articles précédents :
Stratégies thérapeutiques pour les douleurs en lien avec les sacro-iliaques (Partie 1/3)
Stratégies thérapeutiques pour les douleurs en lien avec les sacro-iliaques (Partie 2/3)
Retour à la case départ :
Références : (par ordre d’apparition dans le texte)
- Rousseau L, Bacelon M. Facteurs psychosociaux, douleur et kinésithérapie. Kinésithér Rev 2017 Jun ;17(186):33-43
- Barker KL, Reid M, Minns Lowe CJ. Divided by a lack of common language? A qualitative study exploring the use of language by health professionals treating back pain. BMC Musculoskelet Disord. 2009 Oct 5;10:123
- Darlow B, et al. The Enduring Impact of What Clinicians Say to People With Low Back Pain. Ann Fam Med. 2013 Nov-Dec;11(6):527-34
- Howick J, et al. Effects of empathic and positive communication in healthcare consultations: a systematic review and meta-analysis. J R Soc Med. 2018 Jul;111(7):240-252
- Ferreira PH, et al. The Therapeutic Alliance Between Clinicians and Patients Predicts Outcome in Chronic Low Back Pain. Phys Ther. 2013 Apr;93(4):470-8
- Darlow B, et al. The association between health care professional attitudes and beliefs and the attitudes and beliefs, clinical management, and outcomes of patients with low back pain: A systematic review. Eur J Pain. 2012 Jan;16(1):3-17
- Gardner T, et al. Physiotherapists’ beliefs and attitudes influence clinical practice in chronic low back pain: a systematic review of quantitative and qualitative studies. J Physiother. 2017 Jul;63(3):132-143
- Nickel B, et al. Words do matter: a systematic review on how different terminology for the same condition influences management preferences. BMJ Open 2017;7:e014129
- Smith BE, et al. Should exercises be painful in the management of chronic musculoskeletal pain? A systematic review and meta-analysis. Br J Sports Med. 2017 Dec;51(23):1679-1687
Laisser un commentaire